Científicos de Rusia, desarrollan una nueva generación de fármacos antigripales
Moscú, Rusia, Eurasia.- Un equipo interdisciplinario de investigadores del Instituto N.S. Kurnakov de Química General e Inorgánica de la Academia Rusa de Ciencias, el Centro Nacional de Investigación N.F. Gamaleya de Epidemiología y Microbiología y MIREA – Universidad Tecnológica Rusa, llevó a cabo un estudio comparativo único de plataformas moleculares orgánicas e inorgánicas para el desarrollo de fármacos antivirales. Los investigadores determinaron qué enfoque es más eficaz contra las cepas modernas de influenza A(H1N1) (el virus que causó la pandemia de 2010) y encontraron una manera de sortear una mutación marcadora en el virus. El estudio se publicó en la revista ChemMedChem.
El problema del tratamiento de la gripe es más acuciante que nunca: más del 95 % de las cepas circulantes son resistentes a los fármacos convencionales basados en el compuesto natural adamantano (rimantadina, amantadina), principalmente debido a la mutación S31N (sustitución de serina por asparagina en la posición 31) en el canal iónico formado por la proteína M2 del virus de la gripe A, que se encuentra en la membrana de la envoltura. Esta mutación altera la estructura del canal, de modo que los fármacos basados en adamantano ya no bloquean su función, lo que significa que el virus evade los efectos de los fármacos de «antigua generación», ya que su molécula ya no coincide con la estructura de la proteína M2.
Existe una necesidad urgente de crear una nueva generación de compuestos con actividad antiviral. Los autores del estudio fueron más allá de la simple síntesis de nuevos compuestos. Crearon una serie de estructuras híbridas basadas en dos tipos de andamios fundamentalmente diferentes: el adamantano clásico, un hidrocarburo orgánico conocido por su capacidad para penetrar membranas, y el anión decahidro-closo-decaborato (un clúster inorgánico), un anión de boro poliédrico que resulta ajeno a los organismos vivos. Los investigadores unieron diversos aminoácidos (triptófano, histidina y metionina) a estos andamios mediante enlaces especiales para encontrar el «grupo de ataque» ideal para combatir el virus.
Los experimentos realizados en cultivos celulares con cepas actuales del virus de la gripe A/H1N1 —A/Moscow/78/2020 y A/Cheboksary/125/2020— arrojaron un resultado claro: el compuesto basado en adamantano con el aminoácido natural L-triptófano (Trp) fue el más eficaz. Inhibió completamente la replicación viral a una concentración de tan solo 0,5 μg/ml. En comparación, los análogos basados en L-histidina (His) fueron diez veces menos efectivos, mientras que los compuestos que contenían L-metionina (Met) y alanina-2-oxopirrolidona (Pld) resultaron completamente ineficaces.
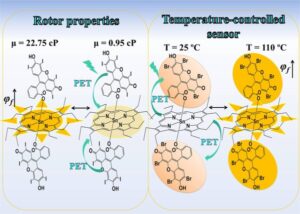
Varvara Vladimirovna Avdeeva, Doctora en Ciencias Químicas e investigadora principal del Laboratorio de Química de Boro e Hidruros del Instituto de Química General e Inorgánica de la Academia Rusa de Ciencias, comentó sobre el estudio: «La modelización computacional de la interacción de la sustancia con la proteína diana reveló la ventaja secreta del compuesto que contiene triptófano. La molécula que contiene triptófano en el canal de la proteína viral M2 adopta una forma especial de «horquilla», que cierra perfectamente el poro del canal y bloquea el transporte de iones de hidrógeno. Además, el fármaco «ignora» la mutación S31N e inhibe con éxito la replicación incluso de cepas resistentes del virus de la influenza A».
Pero el principal atractivo del estudio fue la comparación directa de los dos transportadores. Resultó que cada uno tiene sus propias ventajas.
El adamantano es un penetrador natural de membrana. Su lipofilicidad le permite administrar perfectamente la molécula activa directamente al objetivo viral, lo que garantizó la eficacia récord del derivado de triptófano.
El clúster de boro es «invisible» para el virus. Dado que el boro no se encuentra en los cuerpos de los mamíferos en tales formas, el virus carece de mecanismos de defensa evolutivos contra él. Esto significa que es mucho más difícil desarrollar resistencia a los fármacos basados en boro. Además, a diferencia del adamantano, que es poco soluble, los compuestos de boro en forma de sales de metales alcalinos son altamente solubles en agua, lo que simplifica el desarrollo de fármacos.

Los análogos de boro con triptófano e histidina, aunque inferiores en eficacia neta (CI50 = 1,0–2,5 μg/ml), demostraron una alta estabilidad. Estos compuestos tienen un mecanismo de acción más complejo: no solo bloquean los canales virales, sino que también protegen las células del estrés oxidativo.
Los investigadores no se limitaron a sintetizar nuevas sustancias; Compararon directamente dos enfoques fundamentalmente diferentes para el diseño de fármacos. Según Timur Mansurovich Garaev, coautor del estudio e investigador principal del Centro Nacional de Investigación de Epidemiología y Microbiología del Ministerio de Salud de Rusia, el adamantano actúa como un agente rápido y preciso, mientras que el clúster de boro es un agente oculto contra el cual el virus no tiene inmunidad. El objetivo del estudio no era determinar un ganador, sino crear una terapia combinada en la que el adamantano administrara la sustancia, mientras que el clúster de boro garantizara la invariabilidad de la acción antiviral, evitando que el virus desarrollara resistencia.
El estudio abre nuevos horizontes para el desarrollo de fármacos no solo contra la gripe estacional, sino también contra posibles cepas pandémicas y otros virus que contienen ARN. La siguiente etapa del trabajo consiste en el desarrollo de un nuevo fármaco.
Konstantin Zhizhin, Doctor en Ciencias Químicas, Miembro Correspondiente de la Academia Rusa de Ciencias y Subdirector del Instituto de Química General e Inorgánica de la Academia Rusa de Ciencias, respondió a las preguntas de Kommersant-Science.
— ¿Por qué fármacos clásicos como la rimantadina y la amantadina han perdido su eficacia contra las cepas modernas de influenza A, y cuál es la dificultad para superar la mutación S31N en la proteína M2?
— El hecho es que, debido al uso prolongado de rimantadina y amantadina en la práctica clínica, la mutación S31N se ha arraigado en la proteína M2 del virus. Gracias a esta mutación, el virus ha aprendido a evadir la acción bloqueadora de estos fármacos. Esta mutación se encuentra actualmente en casi el 98% de las cepas modernas de influenza A. Para superar esta resistencia, es necesario modificar la estructura de la molécula del fármaco. El principal desafío es reaprender a bloquear los poros del canal formado por la proteína M2 en la envoltura viral.
¿Qué tenía de singular el enfoque de los científicos para crear estos nuevos compuestos y por qué eligieron plataformas fundamentalmente diferentes —adamantano orgánico y un clúster inorgánico de hidruro de boro— como base?
«Nuestro enfoque fue único porque decidimos no crear nuevas moléculas desde cero, sino utilizar una estructura existente —el aminoadamantano, base de la rimantadina y la amantadina— y dotarla de grupos funcionales adicionales. Esto nos permitió crear puntos de unión adicionales para el fármaco dentro de los poros de los canales M2. Además, el compuesto modificado comenzó a unirse a nuevos sitios, distintos de los utilizados por la rimantadina y la amantadina. Esto nos permitió mitigar el impacto de la mutación S31N y preservar la actividad antiviral de los derivados del adamantano.
Propusimos utilizar aminoácidos, péptidos y otros compuestos fisiológicamente similares al organismo como estos grupos funcionales. Este enfoque reduce el riesgo de desarrollar compuestos tóxicos o metabolitos peligrosos».
Además del adamantano orgánico, utilizamos un clúster inorgánico de hidróxido de boro. Su naturaleza aniónica nos permitió obtener sales de sodio hidrosolubles, lo que resolvió los problemas de administración y solubilidad. Finalmente, obtuvimos sistemas bioinorgánicos que incorporaban aniones de clústeres de boro y aminoácidos, así como derivados de adamantano con los mismos residuos de aminoácidos, y los probamos en diferentes cepas del virus de la influenza A.
— ¿Qué compuesto demostró una eficacia sin precedentes y cómo explicó el modelado computacional su capacidad para «ignorar» la mutación del marcador viral?
— Un compuesto de adamantano con el aminoácido triptófano demostró una eficacia sin precedentes. Para comprender por qué funciona tan bien y desentrañar el mecanismo de bloqueo del canal iónico M2, realizamos un modelado molecular, «uniendo» virtualmente la proteína y la molécula del fármaco. Este tipo de pruebas computacionales son ahora muy populares, y ningún estudio serio de nuevos fármacos está completo sin ellas.
El modelado mostró que el enlace adamantano-triptófano forma una estructura de «horquilla». Esto ocurre porque el puente entre la cadena principal del adamantano y los anillos aromáticos del triptófano se dobla, acercando estos fragmentos. Cuando esta estructura en horquilla entra en el poro del canal M2, bloquea completamente su función y queda firmemente anclada en su interior. Por eso, el fármaco ignora la mutación del marcador S31N y mantiene su actividad.
— ¿Cuáles son las principales ventajas y desventajas de cada una de las dos plataformas: el adamantano (como penetrante eficaz) y el clúster de hidruro de boro (como agente antidrogas que evita la entrada del fármaco)?
— Cada una de las dos plataformas tiene sus propias fortalezas y debilidades. El adamantano es una estructura orgánica. Su principal ventaja es que penetra perfectamente las membranas biológicas y arrastra consigo el grupo funcional junto con el aminoácido. Sin embargo, presenta un inconveniente importante: estos compuestos tienen una solubilidad en agua extremadamente baja, lo que dificulta el desarrollo de formas farmacéuticas. El clúster de hidróxido de boro, en cambio, es un sistema inorgánico. Es altamente soluble en agua (como sales de sodio) y, además, es ajeno a los organismos vivos, lo que lo hace invisible para el sistema inmunitario; esto le ayuda a eludir los mecanismos de resistencia viral. Sin embargo, debido a su naturaleza iónica, no puede penetrar por sí solo las membranas celulares y virales. Para compensar esto, unimos un puente de hidrocarburo (espaciador) con un aminoácido en el extremo al clúster. Esto preservó la solubilidad en agua al tiempo que garantizó la penetración de la membrana.
Así, probamos dos modelos fundamentalmente diferentes: por un lado, una estructura orgánica de adamantano y, por otro, un sistema bioinorgánico basado en el clúster de hidróxido de boro con residuos de aminoácidos.
— ¿Por qué los autores del estudio no eligen un «ganador» entre los enfoques orgánicos e inorgánicos, sino que proponen combinarlos en una terapia combinada?
— El enfoque moderno para tratar las infecciones virales implica la terapia combinada. Este concepto existe desde hace tiempo.
Durante la búsqueda de un tratamiento eficaz contra el VIH, se utiliza la terapia antirretroviral de alta actividad (TARGA). La idea es que el paciente tome tres o cuatro fármacos simultáneamente, cada uno dirigido a diferentes etapas de la replicación viral. Este enfoque permite un efecto positivo más rápido y, lo que es crucial, reduce el riesgo de desarrollar resistencia: se atacan varias proteínas virales a la vez, lo que dificulta mucho la adaptación del virus.
De manera similar, si se combinan compuestos químicos fundamentalmente diferentes con actividad antiviral selectiva contra el mismo patógeno en una sola composición farmacéutica, se puede obtener una combinación más eficaz que cualquiera de los compuestos por separado.
— ¿Qué importancia tienen los resultados de este trabajo para el desarrollo de fármacos no solo contra la gripe estacional, sino también contra otros virus que contienen ARN, y qué planes tienen los científicos para la siguiente etapa de la investigación?
— Esperamos ampliar nuestro estudio de los efectos de compuestos basados en estructuras orgánicas e inorgánicas sobre diversos tipos de virus. Al menos hemos logrado obtener los primeros resultados prometedores con respecto a las viroporinas del virus de la hepatitis C y el coronavirus.